薬理活性、ADME、毒性、物性の特徴
一般的に薬理活性はその作用メカニズムが比較的シンプルできれいであり、複雑な相互関係を有することは殆どない。また、多くの場合はメカニズムが明確になり、その結果ターゲットたんぱく等が固定されて創薬ステップに乗っていることが多い。これに対してADME、特に毒性はメカニズムが不明かつ複雑なことが多い。また、予測という観点でみた場合、ADMEや毒性は予測対象とすべき化合物の構造変化性(多様性)が極めて高いという特徴がある。即ち、メタン、エタンレベルから、テルペン、ステロイド、マクロライド、糖等の基本構造や分子量まで大きく異なる化合物を対象とした予測が求められる。
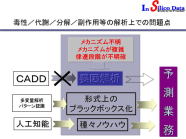
現在適用されている構造-活性相関(QSAR)やドッキング手法では、要因解析を行う都合上このような構造変化性の極めて高い化合物群を対象にした予測は基本原理から実施不可能である。即ち、ADME、毒性、物性の予測は不可能ではないが原理上困難、且つ危険である。 |
 |


